Wundermittel ohne Wirkung
Zahlreiche Infektionskrankheiten, die Menschen Jahrzehnte und Jahrhunderte plagten, gelten heute als kontrollierbar oder sogar weitgehend besiegt. Die medizinischen Errungenschaften der vergangenen rund 150 Jahre waren ein Segen für die Menschheit. Und doch geht der Blick derjenigen, die sich mit Infektionskrankheiten beschäftigen, welche pandemisches Potenzial haben und uns möglicherweise in Zukunft vor große medizinische Herausforderungen stellen, auch in die Vergangenheit. Denn gerade diejenigen Krankheiten, die wir heutzutage als nicht weiter schwerwiegend unterschätzen und auf die leichte Schulter nehmen, könnten in Zukunft in all ihrer Gefährlichkeit zurückkommen – denn wirksame Medikamente könnten bald Mangelware sein.
Antibiotika waren seinerzeit ein großer Durchbruch im Kampf gegen bakterielle Infektionskrankheiten, die weltweit zahlreiche Menschenleben forderten. Mittlerweile hat das Vorkommen von Antibiotikaresistenzen allerdings stark zugenommen und stellt eine Bedrohung dieser medizinischen Errungenschaft dar. Laut einer Hochrechnung der Europäischen Seuchenschutzbehörde ECDC starben im vergangenen Jahr 33.000 Menschen in Europa aufgrund von multiresistenten bakteriellen Erregern (MRE). Jährlich erkranken europaweit rund 670.000 Menschen an Infektionen durch MRE. Deren Behandlung ist nicht nur kostspieliger und dauert länger, auch besteht immer das Risiko, dass der Krankheitsverlauf nicht mehr aufzuhalten ist und tödlich endet.
Bakterien gehören zu den ältesten Lebewesen auf der Erde. In mehreren Milliarden Jahren Evolution haben sie sich entwickelt und immer wieder angepasst. Nicht nur sind sie ein wichtiger Bestandteil des menschlichen Lebens, sondern allen Lebens auf der Erde. Der Mensch wird von mehr Bakterien besiedelt als er eigene Körperzellen hat. Doch einige wenige Bakterien verursachen schwerwiegende Krankheiten beim Menschen oder haben das Potenzial, Infektionen auszulösen.
Antibiotika galten lange als Wundermittel, um diesen Bakterien zu begegnen. Die antibiotische Wirkung kann dabei unterschiedlich sein: Sie kann die Zellwand der Bakterien zerstören, ihre Proteinbiosynthese hemmen oder die Replikation des Erbguts hemmen. Doch immer mehr Bakterien können Antibiotika nichts anhaben. Der Grund liegt auf der Hand: Gerade der breite Einsatz dieser Wundermittel ist es, der ihre Wirksamkeit vermindert. Der evolutionäre Vorteil derjenigen Bakterien, die Resistenzen besitzen, ist enorm, so dass sie sich mittelfristig durchsetzen.
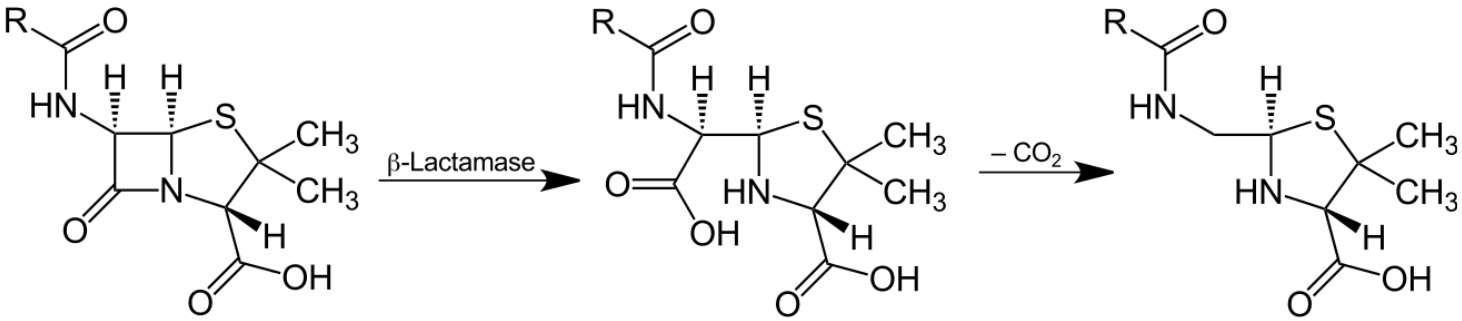
Abb. 1: Eine β-Lactamase katalysiert die hydrolytische Öffnung des Lactam-Vierrings von β-Lactam-Antibiotika, welches
anschließend decarboxyliert und nicht mehr wirksam ist. © www.wikipedia.de
Denn Bakterien entwickeln Mechanismen, um die antibiotischen Substanzen zu zerstören, das Eindringen dieser Substanzen in die Zelle zu verhindern, das Antibiotikum einfach wieder auszuscheiden oder ihre eigene Struktur so zu verändern, dass die Substanzen das Bakterium nicht mehr erkennen. Und nicht nur das resistente Bakterium vermehrt sich, darüber hinaus können Resistenzgene an andere Bakterien weitergegeben werden und so deren Resistenz fördern. Gleich mehrere Resistenzgene, die sie gegen verschiedene Antibiotika schützen, können so aufgenommen werden. Die Folge: multiresistente Erreger.
Im Gesundheitswesen ist der Einsatz von Antibiotika Alltagsgeschäft. Teilweise werden Antibiotika auf Verdacht oder vorsorglich verabreicht. In Krankenhäusern, Pflegeeinrichtungen oder Arztpraxen lassen sich daher vermehrt MRE finden. Ein weiterer Bereich, in dem Antibiotika in großen Mengen eingesetzt werden, ist die Nutztierhaltung. Neben der Schweinemast und Aquakulturen ist vor allem die Geflügelmast stark betroffen. Aufgrund der hohen Dichte der Tierhaltung in den Ställen werden hier Antibiotika häufig eingesetzt. Auch wenn nur einzelne Tiere erkrankt sind, erhalten teils alle Tiere metaphylaktisch Antibiotika, was die Wahrscheinlichkeit, dass sich resistente Keime anreichern, zusätzlich steigert.
Insbesondere TierärztInnen und Personen, die unmittelbar mit Nutztieren in Kontakt kommen, sind gefährdet. Teilweise lassen sich sehr hohe Kolonisierungsraten von MRE bei diesen Personen feststellen. Genauer gesagt von MRSA, also Methicillin-resistenten Staphylococcus aureus. Staphylokokken sind meist harmlos und besiedeln die Haut und Schleimhäute des Menschen. Doch können sie auch pathogen sein und damit eine ganze Reihe von Erkrankungen von Hautinfektionen über Lungen- und Hirnhautentzündungen bis hin zur Sepsis verursachen. Im Normalfall werden diese Staphylokokken mit dem Antibiotikum Oxacillin behandelt – was bei MRSA jedoch keine Wirkung mehr hat. Eine Übertragung von Nutztieren auf den Menschen ist leicht möglich, und auch von Mensch zu Mensch kann der Erreger dann weitergegeben werden.
Wie eng Tier- und Umweltschutz mit der Gesundheit des Menschen verbunden sind, zeigt sich unmittelbar in der Anreicherung antibiotikaresistenter Keime. Die Entwicklung einer gemeinsamen Strategie von Veterinär- und Humanmedizin und dem Öffentlichen Gesundheitsdienst ist schließlich eines der Ziele des Forschungsverbundes #1Health-PREVENT. Darüber hinaus erstellt der Verbund, der Teil des Forschungsnetzes Zoonotische Infektionskrankheiten ist, Studien zur Prävention und Intervention von MRE bei Nutztieren und Begleittieren.
Im Fokus der Untersuchungen stehen dabei mehrere resistente oder multiresistente und biozid-unempfindliche Erreger. Neben MRSA sind hier unter anderem Darmbakterien zu nennen, die β-Laktamasen mit breitem Wirkungsspektrum besitzen (‚Extended spectrum β-lactamase‘) besitzen. Diese Enzyme hydrolysieren das allen β-Lactam-Antibiotika gemeinsame Strukturmerkmal, den β-Lactam-Ring, und macht diese so unwirksam. Darüber hinaus gibt es Carbapenemase-produzierende Enterobacterales (CPE), die die Gruppe der Carbapenem-Antibiotika unwirksam machen, und Colistin-resistente Enterobacterales (Col-E), die unempfindlich gegenüber dem Antibiotikum Colistin sind.
Escherichia coli und andere Bakterien der Ordnung Enterobacterales gehören zum Mikrobiom des Menschen, aber auch zu dem aller Säugetiere, Vögel und Reptilien. Zunehmend vermehren sich unter ihnen jedoch die ESBL-Varianten. Die Übertragung findet fäkal-oral statt, auch von Mensch zu Mensch. Daher sind sie besonders als Infektionserreger in Krankenhäusern verbreitet. Stark belastet sind darüber hinaus die Nutztieranlagen: Zwischen 61 und 85 Prozent der beprobten Schweineanlagen waren in Deutschland belastet, 87 Prozent der Rinderanlagen und bis zu 100 Prozent bei der Geflügelmast. Von den Mastanlagen ist der Weg in die Schlachthöfe und Supermärkte wiederum nicht weit. Vier Prozent der untersuchten Rindfleischproben im Einzelhandel enthielten ESBL-E. coli, bis zu 13 Prozent der Schweinefleisch- und bis zu 75 Prozent der Hähnchenfleischproben.
Zwischen sechs und zehn Prozent der Menschen in Deutschland sind mit ESBL-E. coli besiedelt. Zwar handelt es sich hierbei um eine asymptomatische Besiedlung des Darms, sie stellt jedoch ein Reservoir für später auftretende Infektionen dar. In Südostasien liegt die Besiedlung teilweise bei über 60 Prozent.
Es wird angenommen, dass neben Mensch-zu-Mensch-Übertragungen in Haushalten oder Gesundheitseinrichtungen und neben einem Erwerb bei Fernreisen, auch Tierkontakte und ESBL-kontaminierte Lebensmittel zur Besiedlung des Menschen beitragen. Über die CPE- und Col-E-Besiedlungen liegen bislang für Deutschland nur wenige Daten vor.
Die WHO erstellte vor drei Jahren eine Liste mit den bedeutendsten gegen Antibiotika resistenten Bakterien: auf Platz eins die Carpabenem-resistenten Bakterien, auf Platz zwei die Kategorie zu der auch MRSA zählen.
Über die Ausscheidungen von Masttieren und verschiedene Abwässer gelangen multiresistente Erreger wie MRSA und ESBL-bildende Enterobacterales in die Umwelt, in Böden und Gewässer. Wildtiere und Heimtiere können die Erreger so wiederum aufnehmen und weiterverbreiten. Und natürlich kann auch der Mensch – selbst wenn er nicht erkrankt – resistente Erreger ausscheiden und übertragen.
Letztlich kann die Resistenzbildung nicht aufgehalten wohl aber verlangsamt werden. Damit dies gelingt, müssen viele verschiedene Akteure bewusst und entschieden handeln – und das bestenfalls global.
Quellen:
- „Multiresistente Erreger – ein One Health Problem“, Robin Köck, Caroline Herr, Lothar Kreienbrock, Stefan Schwarz, Bernd-Alois Tenhagen, Birgit Walther (Manuskript)
- „Antibiotikaresistenz. Eine gesellschaftliche Herausforderung“, Esther-Maria Antao, Christian Wagner-Ahlfs (Bundesgesundheitsblatt 2018)
- „Die Jagd nach neuen Antibiotika“, Corie Lok (Spektrum, Juli 2015)
- „Antibiotic resistance: The Last Resort“, Mary McKenna (Nature 499, 2013)
- https://www.rki.de/SharedDocs/FAQ/Krankenhausinfektionen-und-Antibiotikaresistenz/FAQ_Liste.html#FAQId11706058
- https://www.rki.de/DE/Content/Infekt/Antibiotikaresistenz/Uebersichtsbeitraege/AMR_Europa.html
- https://www.rki.de/DE/Content/Infekt/Antibiotikaresistenz/Grundwissen/Grundwissen_inhalt.html
- RAI-Podcast „Schweinecast“, Folge 1